中裕新藥(4147-TW)正積極推動其長效愛滋病療法TMB-365/380的國際授權合作。這一戰略的關鍵在於,該療法在臨床二期試驗中展現了優異的數據,不僅證明其具備成為重磅藥物的潛力,更使其成為全球唯一用於愛滋病治療、且可能顛覆現有治療模式的單株抗體組合『game changer』。因此,尋求與國際大藥廠的合作,加速商業化進程,是中裕新藥(4147-TW)當前最重要的戰略目標。
中裕新藥公司概況
中裕新藥(4147-TW)成立於2007年,是一家專注於愛滋病治療領域的生物製劑開發公司。
其商業模式主要為自研究機構或新藥開發公司引進臨床前或臨床一、二期具潛力藥物,再透過公司團隊的專業能力進行開發和拓展新應用,最後授權適合的藥廠進行國際行銷,從中獲取權利金和上市利益。
目前中裕新藥(4147-TW)已有一項產品TrogarzoTM取得美國FDA的上市許可。
- TrogarzoTM (ibalizumab) 是中裕新藥(4147-TW)的第一個上市產品,這是一種單株抗體生物製劑,主要針對多重抗藥性HIV-1感染的愛滋病患。
- 中裕新藥(4147-TW)於2007年自美國Genentech技轉取得全球市場獨家授權,並持續在美國/台灣進行臨床試驗。
- TrogarzoTM已取得歐、美藥證,並在歐洲、北美及中東等30餘國上市,其市場成功為TMB-365/380的研發和未來商業化奠定了堅實基礎。
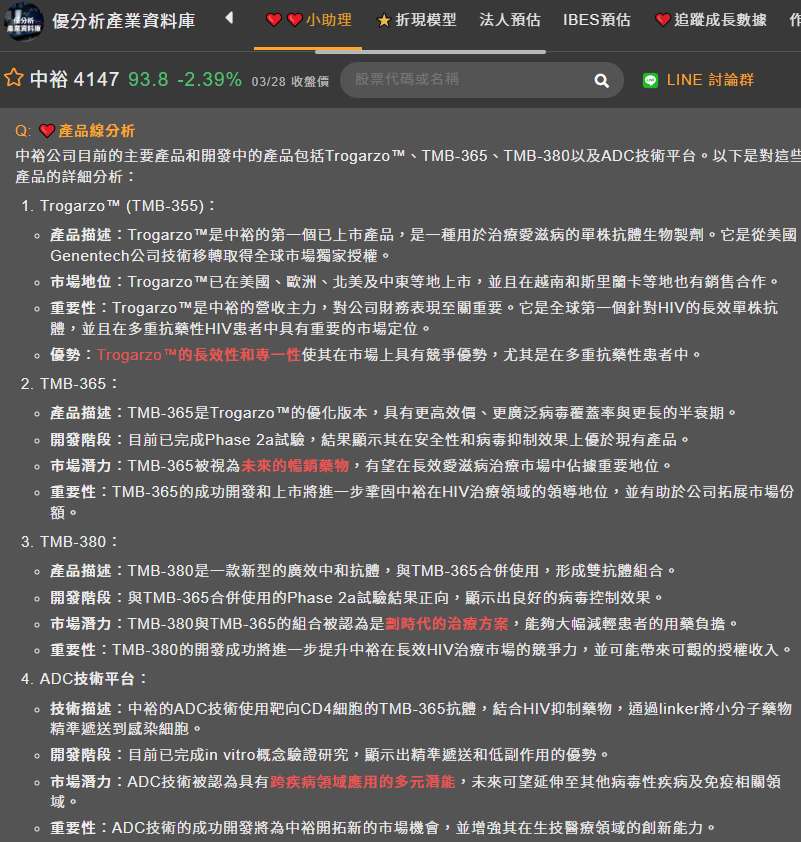
(資料來源:優分析產業資料庫)
愛滋病長效治療市場趨勢
隨著愛滋病治療的進步,長效治療方案也逐漸成為市場的新趨勢。
長效型抗反轉錄病毒藥物已成為HIV感染者備受期待的治療選項。與每日口服療法相比,長效方案可以改善用藥的順從性、便利性、耐受性和成本。
全球愛滋病藥物市場規模預估在2030年可達430億美元,其中長效療法市佔率可望達30%以上,顯示其強勁的成長潛力。
ViiV Healthcare (GSK子公司)於2021年推出長效型肌肉注射愛滋病藥物Cabenuva,因其可免除患者每日服藥的不便,顯著提升用藥順從性、便利性與生活品質,銷售表現優於預期,驗證了市場對長效藥物的強勁需求。
這也意味著,同樣具有長效優勢的TMB-365/380,未來在國際合作談判中將更具優勢。
中裕的單株抗體組合,沒有小分子藥物的藥物交叉作用與肌肉注射的不適感。除此之外,中裕的組合不需似其他同類藥物需做抗藥篩檢,此篩檢將限制患者選擇並延誤治療時機,影響病患權益,中裕產品為同類產品之best-in,也是指日可待的暢銷藥(blockbuster drug)。
(資料來源:優分析產業資料庫)
TMB-365/380臨床數據優異,授權前景可期
- TMB-365為Trogarzo (ibalizumab) 的優化版本,能更有效地與CD4受體結合,阻斷病毒入侵。
- TMB-380則是一款新型的廣效中和抗體 (bNAb),同樣具備長效特性,作用於HIV-1病毒表面的gp120蛋白,降低其感染力。
兩者協同作用,針對愛滋病病毒入侵的不同階段,產生更強大的治療效果,並降低抗藥性風險。
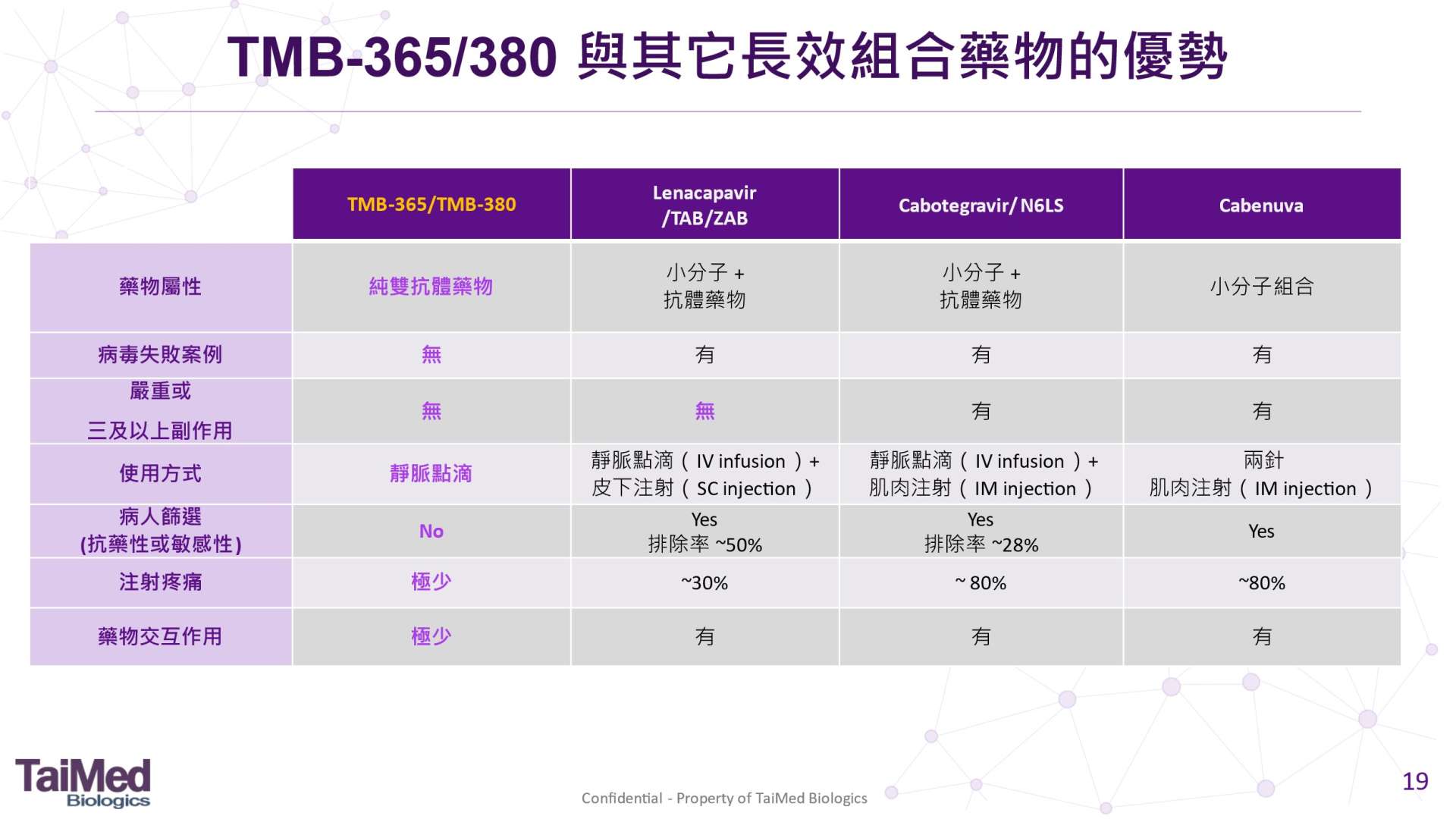
根據 Gilead 與 ViiV 於 CROI 發表之研究數據與中裕公司近日法說簡報,可以觀察到在病毒失敗與安全性表現等,中裕組合較具優勢。
TMB-365/380的二期臨床試驗數據顯示優異的安全性及有效性。原本每日口服聯合抗病毒治療藥物的受試者,在轉換至此方案後,病毒抑制率達到94%,且CD4細胞計數顯著提升,展現了其在愛滋病病毒維持治療中的顯著效果。
在安全性方面,TMB-365/380臨床試驗證實,未有因治療導致任何嚴重或三級以上不良事件;反觀國際大廠之同類療法臨床試驗,部分患者出現三級以上的不良事件,再次顯現中裕新藥(4147-TW)產品於藥物安全上的優勢。
TMB-365/380憑藉其優異的臨床數據、龐大的長效治療市場潛力,以及相對於競爭產品的安全性優勢,已具備極高的授權價值。正如執行長張金明所說,中裕新藥(4147-TW)將積極與國際大藥廠展開授權合作,加速TMB-365/380的商業化進程,為公司創造可觀的營收和利潤。
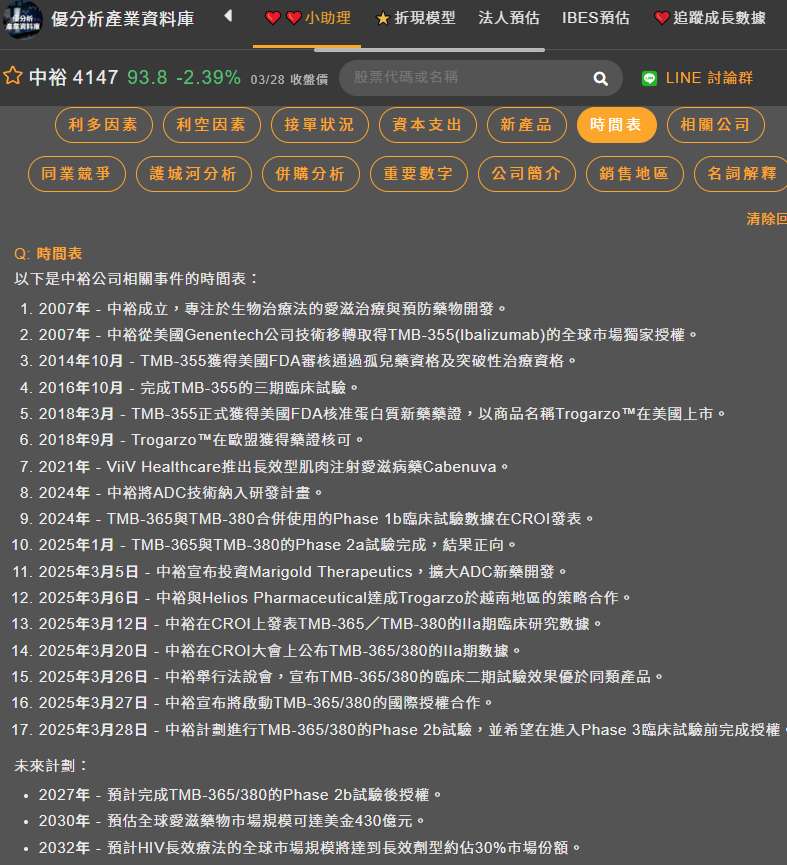
(資料來源:優分析產業資料庫)
積極與國際大藥廠或夥伴合作
未來,中裕將啟動與美國FDA討論2b階段試驗設計。
也將以優異的2a期臨床試驗結果,積極與國際大藥廠或全球策略性夥伴探討潛在授權與共同開發之機會,加速商品化進程,進一步擴大中裕企業價值與國際影響力。